Nach dem Stich einer infizierten Mücke gelangen Plasmodien schnell mit dem Blutstrom in die Leber und vermehren sich dort unerkannt („Leberphase“). Man nahm an, infizierte Leberzellen würden schließlich platzen und die Parasiten ins Blut entlassen. Was hier so simpel klingt, war seit der Entdeckung des Malaria-Parasiten vor 130 Jahren unerforschtes Gebiet: Wie kann es den relativ unbeweglichen Parasiten gelingen, aus dem Lebergewebe durch die Wände der Blutgefäße zurück in die Blutbahn zu finden?
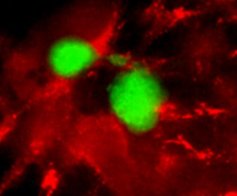
Heussler und Kollegen wiesen nach, dass Malaria-Parasiten nach mehreren Tagen in der Leber den Tod ihrer Wirtszellen einleiten. Mit Hilfe gentechnisch veränderter, grün leuchtender Parasiten konnten sie beobachten, dass die infizierten Leberzellen kleine Membransäckchen ausbilden. Die Membransäckchen wurden von den Wissenschaftlern „Merosomen“ getauft.
Die Parasiten werden von der Zelle in die Merosomen gepumpt und so verpackt in die Blutbahn geschleust (Science 2006, Band 313, S. 1287 – 1290). Die Merosomen funktionieren wie ein trojanisches Pferd: Die so umhüllten Parasiten werden von den zahlreichen Fresszellen der Leber nicht als Eindringlinge erkannt. So gelangen die Parasiten aus dem Lebergewebe sicher zurück in die Blutbahn. Dort angekommen, zerstören sie das Merosom, werden frei gesetzt und beginnen mit der Infektion roter Blutkörperchen. Der Übergang in diese „Blutphase“ markiert den Beginn der Malaria-Erkrankung.
Verstehen und den Spieß umdrehen
Mit der Entdeckung der Merosomen ist nun der letzte unbekannte Schritt im komplexen Lebenszyklus des Malariaparasiten aufgeklärt. Die Erkenntnisse über den kontrollierten Zelltod der infizierten Leberzellen können helfen den Spieß umzudrehen und Schwachpunkte des Parasiten für die Krankheitsbekämpfung zu nutzen. Gelänge es beispielsweise, die Merosomenbildung zu verhindern, so bliebe der Parasit in der Leberzelle gefangen. Dort überlebt er nur noch wenige Stunden. Bringt man den Parasit auf diese Weise schon in der Leber zum Scheitern, so entsteht aus der Parasiteninfektion keine Krankheit. Eine solche Strategie würde angesichts der rund 300 Millionen Malariafälle pro Jahr dringend gebraucht.
Dr. Volker Heussler (45) studierte Biologie an der Universität Karlsruhe. Nach seiner Doktorarbeit am Institut für Parasitologie in Bern (Schweiz) arbeitete er von 1993 bis 1996 als Postdoktorand am International Livestock Research Institute (ILRI) in Nairobi (Kenia). Danach war er als Junior-Gruppenleiter am Institut für Tierpathologie der Universität Bern tätig, wo er 2002 im Bereich Parasitologie und Zellbiologie habilitierte. Seit 2002 leitet er eine Malaria-Arbeitsgruppe am Bernhard-Nocht-Institut für Tropenmedizin in Hamburg.
Die GlaxoSmithKlineStiftung verleiht jährlich Wissenschaftspreise für medizinische Grundlagenforschung und für klinische Forschung. Die Preise sind mit insgesamt bis zu 30.000 Euro dotiert. Sie prämieren wissenschaftliche Arbeiten, die aktuell, im Forschungsansatz originell und für den biomedizinischen Fortschritt bedeutend sind.