Dynamische Marktentwicklung weltweit und in Deutschland
Biopharmazeutisch hergestellte Arzneimittel wurden seit ihrer Einführung in den 80er Jahren kontinuierlich weiterentwickelt. Auf erste rekombinante Präparate[1] folgten komplexere monoklonale Antikörper[2] und in Zukunft ist mit neuartigen Technologien zu rechnen, die zu einer Änderung der Behandlungsparadigmen führen könnten. Die ersten Biosimilars, also Nachbauten, wurden Mitte der 2000er Jahre eingeführt. Soviel Innovation drückt sich in Umsatzsteigerung aus. Daher zeigt sich die Marktentwicklung der letzten Jahre bis heute sehr dynamisch und der Blick auf die Forschungspipeline lässt eine ebensolche Entwicklung für die Zukunft erwarten wie Analysen von QuintilesIMS nahelegen.
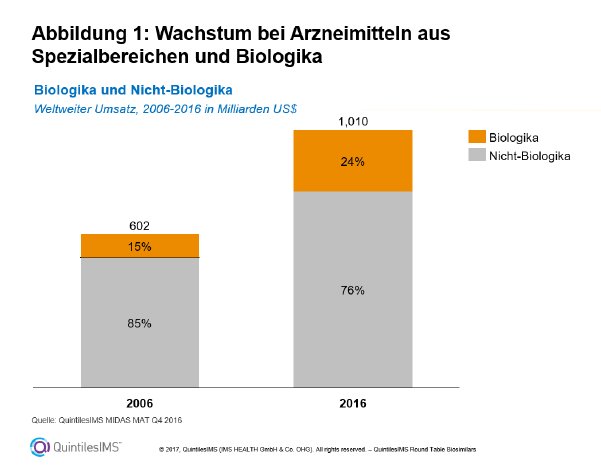
Der globale Biologikamarkt erreichte im Jahr 2016 einen Gesamtumsatz von 246 Mrd. US Dollar (Basis: Herstellerabgabepreis ohne Abzug von Nachlässen und Rabatten). Das bedeutet seit 2006 ein Jahreswachstum von etwa 10 %. Demgegenüber lag der durchschnittliche Zuwachs des nicht-biologischen Segments bei etwa 4 %. Vor diesem Hintergrund entfällt inzwischen fast ein Viertel des weltweiten Umsatzes mit Arzneimitteln auf Biopharmazeutika. Diese Entwicklung gründet sich vor allem auf Spezialbereiche, in denen Fachärzte die innovativen Präparate für die Behandlung komplexer, oftmals chronischer Erkrankungen verordnen (Abb. 1 zum Herunterladen). Ein bekanntes Beispiel für den Fortschritt durch Biologika bilden Arzneimittel zur Therapie von Hepatitis C. Die schwere Viruserkrankung lässt sich dank der neuen Präparate bei den meisten Patienten sogar heilen.
Der größte Wachstumsbeitrag nach Regionen entfällt im internationalen Kontext auf die USA, die 59 % Marktanteil auf sich vereinen und gut zwei Drittel des Wachstums erzeugen.[3]
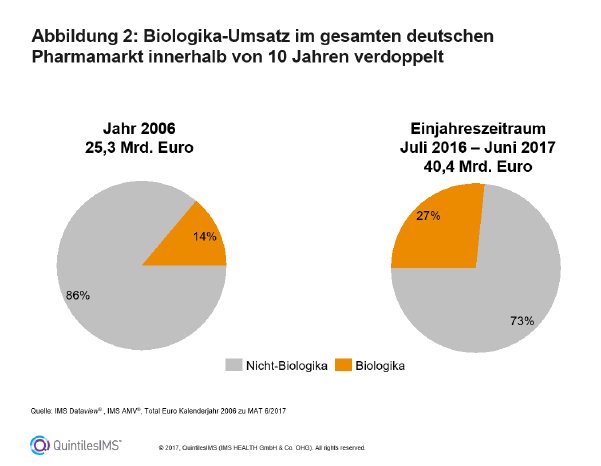
Die dynamische weltweite Entwicklung lässt sich auch für Deutschland nachzeichnen, indem sich der Marktanteil biologischer Arzneimittel im gesamten Pharmamarkt (Apotheken- und Kliniksegment) hierzulande innerhalb von zehn Jahren fast verdoppelt hat und im Einjahreszeitraum Juli 2016 bis Juni 2017 ein Volumen von 10,9 Milliarden Euro (Apothekensegment: Abgabepreis des pharmazeutischen Unternehmers, ohne Abzug jeglicher Rabatte, Kliniksegment: berechnete Preise) erreicht (Abb. 2 zum Herunterladen).
Gut gefüllte Forschungspipeline
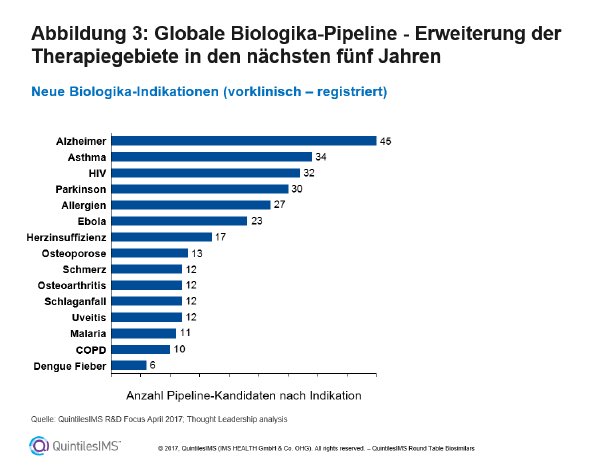
Derzeit werden Biopharmazeutika im Schwerpunkt noch bei Krebs-, Autoimmun- und Stoffwechselerkrankungen eingesetzt, wozu auch seltene Erkrankungen gehören. Aufgrund der Spezifität der Therapeutika sind diese oftmals nur für kleinere Patientenpopulationen indiziert. Die gut gefüllte Forschungspipeline zeigt eine Erweiterung hin zu Erkrankungen, die bislang vor allem mit nicht-biologischen Arzneimitteln behandelt wurden. Darunter finden sich auch hoch prävalente Therapiegebiete wie zum Beispiel Asthma oder Allergien (Abb. 3 zum Herunterladen). Die Entwicklung biopharmazeutischer Medikamente zielt hier auf die Therapie schwerer Fälle ab.
Der zukünftige Markteintritt entsprechender Präparate bedeutet eine Anwendung auch in der Primärversorgung, die bislang durch den Einsatz vor allem niedermolekularer Substanzen charakterisiert ist. Die Versorgung der betroffenen Patienten steht dann der Behandlung mit bewährten Therapeutika, vielfach generischer Herkunft, gegenüber. Ihr Einsatz wird sich am Therapieerfolg, aber auch an den Behandlungskosten bemessen.
Erweiterter Marktzugang durch Biosimilars
Bei allem Therapiefortschritt, den Biologika mit sich brachten, betrachten Kostenträger die Entwicklung mit Blick auf die Finanzierbarkeit als Herausforderung. Deshalb wird „Biosimilars“ eine bedeutsame Rolle zugeschrieben. Durch ihre Markteinführung entstehen Einsparungen und es wird ein breiterer Zugang zu Biologika ermöglicht. Dies auch vor dem Hintergrund, dass in diesem und in den nächsten Jahren die Patente umsatzstarker Originalpräparate auslaufen. In Deutschland verlieren in den nächsten fünf Jahren biologische Originalpräparate im Wert von 2,8 Mrd. Euro ihren Patentschutz. Bei den schon am Markt befindlichen Biosimilars fielen die Preisreduktionen je nach Substanz und Land unterschiedlich aus, was u.a. mit der Angebotsbreite zusammenhing. In den „TOP 5“-Ländern Europas (Deutschland, Frankreich, Italien, Spanien, Großbritannien) sanken die Preise bspw. für das Blutersatzprodukt Epoietin um zwischen 13 und 55 %, für das Wachstumshormon G-CSF zwischen 4 und 27 %.
Die Marktpenetration der Nachbauten zeigt sich im Ländervergleich unterschiedlich, was wesentlich mit gesundheitspolitischen Rahmenbedingungen zusammenhängt. So stellen Ausschreibungen einen wichtigen Einflussfaktor für eine hohe Marktdurchdringung dar. Mit zunehmender Erfahrung erfolgen jedoch auch Änderungen in den Verordnungsempfehlungen von Fachinstitutionen, indem Patienten nicht mehr nur wie zu Beginn auf similare Therapien neu eingestellt, sondern inzwischen auch umgestellt werden sollen. Die Akzeptanz durch die Verordner stellt damit einen weiteren wichtigen Bedingungsfaktor für die Marktdurchdringung dar wie auch die Produktdifferenzierung[4] eine Rolle spielt.
Im Vergleich nach Regionen entfällt der Löwenanteil des Biosimilar-Umsatzes mit vier Fünfteln auf Europa. Allein 62 % davon werden in den „TOP 5“-Ländern erwirtschaftet. In den USA hingegen spielen Biosimilars mit einem Marktanteil von 4 % noch keine große Rolle.
Neue Therapieklassen
Der Fortschritt der biopharmazeutischen Entwicklungen erstreckt sich nicht allein auf Erweiterungen bei Therapiebereichen, sondern auch auf innovative Technologien. Zurzeit[5] dominieren noch monoklonale Antikörper. Die Biologika-Pipeline besteht jedoch schon zu 20 % aus innovativen Technologien wie z.B. Gen-, Zell- und RNAi-Therapien[6]. Auch wenn deren Markteintritt noch nicht unmittelbar bevorsteht, so verweist der Stand der Forschung auf mögliche zukünftige Therapiepotenziale.
Einblicke in die internationale Pharmamarktentwicklung auf der CPhI
QuintilesIMS wird die Entwicklung des Biologikamarktes weiter verfolgen. Auf der Messe CPhI (https://www.cphi.com/europe/), die vom 24. bis 26. Oktober in Frankfurt/Main stattfindet, ist QuintilesIMS mit einem Stand (No. 42C11) vertreten und gibt dort u.a. Einblicke in Analysemöglichkeiten des Weltpharmamarktes. Die Messe deckt ein breites Spektrum pharmazeutischer Themen ab, vom Herstellungsprozess über den Ursprung von Wirkstoffen bis hin zu Produkten und Dienstleistungen, die die gesamte Lieferkette betreffen.
[1] Definition: Durch genetische Modifikation hergestellt, wobei die kodierende DNA für das benötigte Produkt h mit Hilfe eines Plasmids oder viralen Vektors in einen geeigneten Mikroorganismus oder eine geeignete Zelllinie eingeführt wird, in denen diese DNA exprimiert und in Protein translatiert wird. Das gewünschte Produkt wird dann durch Extraktion und Reinigung gewonnen.
2 Definition: Antikörper, die von einer Zelllinie produziert werden, die auf einen einzigen B-Lymphozyten zurückgeht.
3 Anteil am 5-Jahreswachstum von 2012 bis 2016
4 Beispielmerkmale: Anwendungshäufigkeit und -art
5 Zugrunde gelegte Stadien: Phase II bis registriert. Quelle: QuintilesIMS R&D Focus April 2017; Thought Leadership analysis
6 Gentherapie: Einschleusen von genetischem Material in Zellen des Patienten; Zelltherapie: Injektion humaner Zellen in den Körper des Patienten; RNAi: RNA-Interferenz, RNA-Moleküle übersetzen genetische Information aus der DNA in die Bildung von Proteinen und können Gene auch „abschalten“